Gherardi : Mediatic story (2 ou 3 vérités embarrassantes sur ses études)
Publié le 13 Octobre 2017
Assez régulièrement, le professeur Romain Gherardi parle de ses études dans les médias. Dernièrement, sur l'antenne de RMC, Jean-Jacques Bourdin lui demandait si les adjuvants dans les vaccins étaient neurotoxiques. Sa réponse a été (voir ici à 8'30''):
"Chez l'animal, ils sont neurotoxiques. Il n'y a aucune espèce d'hésitation à le dire."
Voici donc une affirmation qui ne laisse aucune place à l'ambiguïté. Pour être aussi affirmatif, il dispose certainement des meilleurs arguments, des études les plus parlantes! Pour le vérifier, lisons la dernière étude à laquelle il a participé: "Non-linear dose-response of aluminium hydroxide adjuvant particles: Selective low dose neurotoxicity", disponible ici et publiée dans la revue "Toxicology". Il s'agit d'une étude sur la souris.
Le contexte
Gherardi est un des principaux défenseurs de l'hypothèse du lien entre les adjuvants aluminiques dans les vaccins et une maladie qu'il a appelée dans un premier temps "myofasciite à macrophages". Régulièrement, des experts font le point sur la littérature, y compris les études de Gherardi :
- Le Comité consultatif mondial de la Sécurité vaccinale (GACVS, OMS) dont la première réunion s’est tenue les 14-15 septembre 1999 et dont le premier rapport a traité de la myofasciite à macrophages. Le GACVS s'est encore penché sur la question en 2002, en 2003, en 2004, avec un résumé sous forme de questions/réponses en 2008),
- l'Académie Nationale de Médecine en 2012,
- le Haut Conseil de Santé Publique en 2013,
- l'Académie Nationale de Pharmacie en 2016.
Il en ressort que les symptômes de cette maladie restent vagues (fatigue chronique, troubles neurologiques,...). Le nombre de cas recensés est limité géographiquement, presque la totalité en France et identifiés par l'équipe de Gherardi. La déclaration des cas est également limitée dans le temps : 445 cas depuis 1995 (alors que l'aluminium est utilisé comme adjuvant depuis plus de 80 ans) et un seul cas survenu depuis 2012 (la date de déclaration peut être différente de la date de survenue). Alors que pour la même période, environ 160 millions de doses de vaccins contenant un adjuvant à base d'aluminium ont été administrées et qu'actuellement environ 12 millions de doses de vaccins contenant un adjuvant aluminique sont administrées chaque année en France.
Les experts reconnaissent l'existence de la myofasciite à macrophages comme une lésion étant une sorte de "tatouage" vaccinal. En gros, de l'aluminium vaccinal peut demeurer au site d'injection du vaccin et on peut ensuite l'observer grâce à une biopsie, comme celles que Gherardi a pratiquées sur ses patients. Selon Gherardi, chez des personnes prédisposées, une partie de cet aluminium peut sur le long terme quitter le site d'injection, atteindre le cerveau et y exercer une activité neurotoxique résultant en la maladie "myofasciite à macrophages". L'équipe de Gherardi préfère maintenant parler de ASIA ("Autoimmune/inflammatory syndrome induced by adjuvants"), peut-être pour éviter la confusion avec la lésion vaccinale.
Mais peu importe le nom utilisé, les rapports d'experts concluent que les études ne permettent pas d'affirmer un lien entre l'adjuvant vaccinal et les troubles neurologiques présentés par les patients suivis majoritairement à Créteil par l'équipe de Gherardi. Ils mettent en garde contre une baisse de la couverture vaccinale, en l'absence de justification scientifique.
En fait, l'aluminium est bien neurotoxique, c'est connu, notamment suite à des études faites sur des insuffisants rénaux hémodialysés (voir le rapport du HCSP) mais les doses utilisées dans les vaccins ne sont pas comparables. Gherardi a une hypothèse : la relation entre la neurotoxicité de l'adjuvant et la dose administrée ne serait pas linéaire. Peut-être que cette étude sur les souris apporte de nouveaux éléments. Voyons de plus près...
Financement et conflits d'intérêts
Les auteurs de l'étude ne déclarent aucun conflit d'intérêts ("competing interests"). Pourtant, Gherardi entretient des liens étroits avec l'association E3M. Cette association regroupe des personnes atteintes de ce qu'elles appellent donc "myofasciite à macrophages", soutenant que leur pathologie est causée par les adjuvants aluminiques. Cette association a participé au financement des études de Gherardi à hauteur de 80 000 euros. Sans compter le lobbying de l'association auprès de l'ANSM pour financer aussi les travaux du chercheur (à hauteur de 150 000 euros). Notons que ces sommes ne sont pas énormes pour de la recherche. Il n'est pas question ici de prétendre qu'il y a une histoire de gros sous derrière ce lien. Il faut simplement reconnaître que la proximité entre le chercheur et l'association est indéniable.
En fait, nous, on doit l'avouer... on s'en moque un peu que ces liens ne soient pas déclarés dans l'article. D'abord, parce qu'on le savait déjà, mais aussi parce que ça ne veut pas forcément dire que l'étude est mauvaise pour autant. On va la lire avant de juger. Mais c'est cocasse, au vu de la vision de E3M concernant les conflits d'intérêts. Dans ce document de 2015, on assiste ainsi à la mise au pilori de ceux qui ne sont pas d'accord avec l'association, en dénoncant leur "proximité intellectuelle et financière" avec l'industrie pharmaceutique.
Si on appliquait les critères de E3M, on pourrait alors dire que "La proximité intellectuelle et financière de Gherardi avec l'association E3M n'est pas un gage d'indépendance lorsqu'il s'agit de se prononcer sur l'origine d'une maladie qui est une certitude pour ceux qui financent une partie de ses travaux".
Pour cette étude en particulier, les auteurs mentionnent trois sources de financement:
- L'ANSM (Agence Nationale de Sécurité du Médicament),
- le CMSRI (Children’s Medical Safety Research Institute),
- et l'université British Columbia Vancouver (Luther Allyn Dean Shourds Estate)
Le CMSRI est une émanation de la "Dwoskin Family Foundation", une association antivaccinaliste (qui se définit plutôt comme "pour des vaccins plus sûrs", évidemment). Gherardi siège au "scientific advisory board du CMSRI (de même que Exley et Shaw, deux des auteurs de l'étude). Le CMSRI, c'est le genre à affirmer que Wakefield est une victime et non un escroc. Du coup, on en arrive à des situations surréalistes dans lesquelles Gherardi et Wakefield sont invités à s'exprimer au cours d'une même conférence (en Jamaïque par exemple, mais après on va râler parce que l'industrie pharmaceutique paierait les vacances des médecins, déguisée en conférences et séminaires, tout ça tout ça...), conférence subsidiée par le NVIC (National Vaccine Information Center, la ligue antivax US), elle-même en lien étroit avec... la Dwoskin Foundation !
L'université British Columbia Vancouver est mentionnée parce que c'est là, dans le département d'ophtalmologie (oui oui !) que travaille Christopher Shaw, un des auteurs de l'étude. Ce n'est pas l'université qui finance mais le fond privé "Luther Allyn Dean Shourds Estate" qui est aussi à tendance antivaccinaliste et qui finance Shaw.
Délai d'acceptation
Le délai moyen d'acceptation pour les articles de la revue Toxicology est d'environ 3 mois : le temps que l'article soit assigné à un membre du bureau éditorial, que celui-ci recrute deux reviewers, que ceux-ci renvoient leurs remarques, que le bureau éditorial les renvoie aux auteurs, que ces derniers répondent aux remarques, que le bureau prenne une décision ou renvoie à nouveau l'article aux reviewers, et ainsi de suite...
Par contre, certains articles sont acceptés très lentement, ou très rapidement, comme c'est le cas de l'article sur les souris (18 jours !). De façon générale, un délai si court peut poser question. Est-ce que les reviewers ont réalisé leur travail méthodiquement? Ou est-ce que, hasard du calendrier, tout le monde était disponible au bon moment ?
L'étude
Tout d'abord, il s'agit d'une étude sur un animal, la souris. Les conclusions d'études animales ne sont pas systématiquement applicables à l'humain mais cela peut ouvrir certaines pistes. Il faut donc être vigilant à ne pas extrapoler excessivement les résultats à l'humain. Les auteurs et Gherardi en sont conscients.
Les groupes et les doses
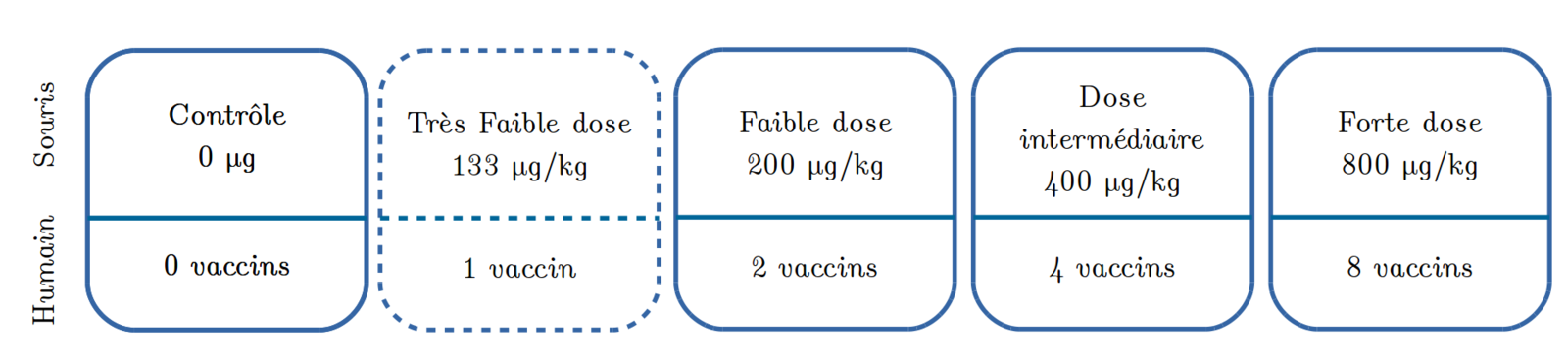
L'étude est réalisée sur 4 groupes de 10 souris. Un groupe témoin et trois autres groupes qui reçoivent des doses différentes d'adjuvants (200, 400 et 800 µg/kg) choisies comme étant équivalentes à 2, 4 et 8 doses de vaccins avec adjuvant aluminique chez l'humain.
Quelques remarques sur ces doses :
- La conversion des doses de l'homme à la souris ne se base pas sur le poids des uns et des autres, il s'agit d'un calcul basé sur la surface corporelle. Ce n'est pas une erreur. Il s'agit même de la conversion recommandée par l'Agence française du médicament. Bon point.
- A l'origine, il existait un cinquième groupe : dose de 133 µg/kg, équivalent à environ 1 vaccin humain. Ce groupe n'est pas mentionné dans l'article (soumis en novembre 2016), mais on en retrouve la trace dans une présentation donnée lors de la "6ème journée d'étude du pôle Santé & Société", à l'université Parie-Est en mars 2016.
- Les doses sont administrées en 3 fois aux souris, quelque soit le groupe. Donc les souris reçoivent leur dose totale d'adjuvant en 3 fois, alors que du côté humain, cette dose totale serait reçue en 2, 4 ou 8 fois. Dit autrement, les souris reçoivent à chaque injection l'équivalent de 2/3, 4/3 ou 8/3 de la dose présente dans un vaccin humain. Ca ne serait pas un problème si c'était bien un effet de la dose totale qui était mis en évidence par l'étude. Mais...
... Spoiler alert : Les auteurs vont conclure que les souris du groupe 200 sont plus affectées par l'aluminium que les souris des groupes 400 et 800, ce qui est contre-intuitif si on a le réflexe de penser en termes de relation linéaire entre la dose et l'effet. Leur hypothèse est que la quantité d'adjuvant présente dans une injection (et non la dose totale reçue après les 3 injections) détermine la toxicité car elle influe sur la possibilité pour les particules de s'agréger ou non entre elles, et donc sur leur possibilité d'atteindre le cerveau. Au final, le protocole qui visait à tester la dose totale n'était peut-être pas adapté. Evidemment, il aurait été difficile d'établir un protocole parfait a priori. A posteriori, l'expérience pourrait être refaite avec un autre protocole défini pour tester l'effet de la taille des agglomérats plutôt que la dose totale. C'est ce qui est suggéré en fin d'abstract. - L'intervalle de temps entre les doses pour les souris n'est peut-être pas représentatif de l'intervalle entre les doses reçues par un humain. Mais si ce n'est pas la dose totale qui importe, alors ce point est probablement sans importance.
Les tests comportementaux
Après 180 jours, un examinateur fait passer 8 tests comportementaux à chaque souris. Nous pouvons lire qu'il s'agit toujours du même examinateur, mais il n'est pas précisé si cela a été fait en aveugle (c'est-à-dire si l'examinateur sait à quel groupe appartient la souris qu'il observe). Si cela n'a pas été fait en aveugle, on ne peut exclure des biais d'observation dans les résultats. Par la suite, les souris seront sacrifiées pour analyses ultérieures.
Nous n'allons pas décrire en détails ces tests comportementaux (lisez l'article). Il faut simplement retenir que chaque test peut lui-même être subdivisé en plusieurs sous-tests. Ainsi le premier test ("open field") compte 7 sous-tests et est destiné à observer la motricité et l'anxiété des souris. Dans l'illustration ci dessous, nous représentons chaque test par un grand rectangle et chaque sous-test par un petit carré. Au final, il y a eu 36 sous-tests (pour 40 souris, ce qui fait quand même 1440 observations pour l'examinateur). Ici, pour parler du second sous-test du premier test, par exemple, nous utiliserons une notation du type T1-2.
Comment sait-on que le résultat d'un test est significatif ou pas?
1) On vérifie si les 4 groupes sont similaires par rapport à ce qui est testé ou pas. C'est ce qui se cache derrière le terme barbare "Anova". Par exemple, pour le T1-1, la quantité p inférieure à 0.05 indique que les 4 groupes ne sont pas similaires et donc le résultat est significatif. Pour le T1-2, p est plus grand que 0.05, ce qui signifie que les 4 groupes sont similaires et le résultat est non significatif (n.s.). Sur les 36 sous-tests, 30 sont non significatifs.
2) Reste 6 sous-tests (T1-1, T1-3, T1-4, T1-5, T1-7 et T5-2) à examiner plus en détails. A ce stade, il faut comparer les groupes entre eux pour déterminer ce qui les rend différents.
- Dans le cas du T1-1, le groupe 200 diffère significativement du groupe contrôle (il diffère donc aussi des groupes 400 et 800 qui sont similaires au groupe contrôle). Ces résultats sont présentés en Figure 1 (a) de l'article. Nous avons donc attribué la notation (a) au petit carré correspondant dans notre illustration ci-dessus pour vous aider à suivre. La situation est similaire pour 3 autres sous-tests du premier test qui sont représentés par les lettre (b, c, d) sur la figure 1 de l'article. Ces 4 sous-tests (T1-1, T1-4, T1-5, T1-7) indiquent donc un effet de l'adjuvant reçu à faible dose (200) tandis que tout va bien lorsque la dose est plus élevée.
- Le T1-3 est significatif mais n'a pas été discuté dans l'article. Nous avons traçé la figure correspondante ci-dessous. On peut raisonnablement supposer que le test est ressorti significatif à cause de la différence entre les groupes 200/400 et le groupe 800. Difficile de dire si la différence entre les groupes 200/400 et le groupe contrôle était significative ou non.
Enfin, reste T5-2 (aussi noté "e" sur la figure 1 de l'article). Il est ressorti significatif mais pas à cause de la différence entre le groupe contrôle et le groupe 200. Au vu de la figure 1(e), c'est la différence entre le groupe 200 et le groupe 400 qui a permis au sous-test de sortir significatif. D'ailleurs, les auteurs parlent de "tendance" entre le groupe 200 et le groupe contrôle et non de différence significative.
Pourquoi mettre en avant T5-2 mais pas T1-3 ? On ne peut pas répondre à la place des auteurs. Mais on ne peut s'empêcher de remarquer que cette "tendance" de T5-2 vient bien commodément s'ajouter aux résultats de T1-1, T1-4, T1-5 et T1-7 pour tenter de renforcer la conclusion que SEUL le groupe 200 est atteint tandis que les résultats de T1-3 vont à l'encontre de cette conclusion. T1-3 met les groupes 200 et 400 au même niveau. La conclusion est donc moins robuste qu'il n'y paraît au premier abord. Et les propos de Gherardi au micro de Bourdin semblent bien péremptoires s'il se base sur des études telles que celle-ci.
Finalement, on remarque qu'on a quand même 30 sous-tests qui disent "rien à signaler", pour seulement 4 sous-tests qui disent "attention à la faible dose" et 2 sous-tests difficilement interprétables. A ce stade, on ne peut même pas vraiment exclure la possibilité que les résultats significatifs puissent être (tout ou en partie) le fait du hasard.
Par exemple, si vous faites plusieurs séries de 10 lancers de pièce, au bout d'un moment, vous allez tomber sur des séries avec un grand écart entre le nombre de piles et de faces qui pourraient laisser croire que la pièce est truquée alors qu'elle ne l'est pas. Ce sont des artefacts statistiques. C'est le problème des tests-multiples. Le problème pourrait empirer lorsque l'on commence à faire des comparaisons entre les groupes au sein des différents sous-tests (6 comparaisons possibles puisque 4 groupes), c'est pourquoi les auteurs utilisent à ce stade un outil adapté pour ces comparaisons (c'est ce qui se cache derrière le terme barbare de "Bonferroni"). On ne peut donc exclure le fait que l'effet significatif de départ soit un artefact statistique. Il reste que le problème des 36 tests effectués sur 40 souris demeure.
Par ailleurs, il est possible que certaines observations aient été réalisées sans que leurs résultats ne soit indiqués dans l'article. Nous avons déjà parlé du groupe "133" absent de l'étude publiée, mais il y a peut-être aussi des tests manquants. Par exemple, dans la description du premier test ("open field"), il est dit que le nombre de fois où la souris se dresse sur ses pattes arrières ("number of rearing") est enregistré. Mais aucune trace de ces observations dans le tableau 1. C'est étrange, surtout si on remarque que cette observation a été faite aussi pour le second test et est bien mentionnée dans les résultats (à retrouver dans le "supplementary data").
Enfin, certains résultats de l'article dans sa version publiée ne sont pas cohérents avec ceux présentés en mars 2016. La présentation indiquait un effet significatif pour le test T2-2 ("elevated O-maze, time spent in open arms") et le test T7-3 ("Tail suspension test, latency to be immobile"). Ces effets se sont perdus en cours de route...
Analyses : les cellules microgliales
Il est annoncé au départ que la moitié des souris (5 dans chaque groupe) doivent servir pour des analyses histologiques des cerveaux. On apprend plus loin que seulement trois de ces cerveaux ont été utilisés, sans qu'on sache trop pourquoi. Par contre, il est cette fois précisé que les analyses sont réalisées en aveugle (la personne qui analyse ne sait pas de quel groupe vient le cerveau analysé).
Il est question d'observer la densité en cellules microgliales (ces cellules ont un rôle dans la gestion des déchets au niveau du système nerveux central, on peut donc supposer que si l'adjuvant migre vers le cerveau, ces cellules seront activées) et la taille de ces cellules et ce dans 4 régions du cerveau ("ventral forebrain", "inferior colliculus ", "visual cortex", "motor cortex"). Donc, on a ici 8 sous-tests.
La taille des cellules est la même pour les 4 groupes (contrôle, 200, 400, 800), quelque soit la région du cerveau considérée. La densité en cellules dans les régions "inferior colliculus", "visual cortex" et "motor cortex" était similaire dans les 4 groupes également. Les résultats ne sont pas communiqués (ni dans le texte principal, ni dans le supplementary data), ce qui n'est pas spécialement dérangeant puisqu'il n'y avait rien de spécial à signaler.
Reste la densité dans la région "ventral forebrain", impliquée dans l'anxiété. Les groupes contrôle et 200 sont significativement différents (plus de cellules pour le groupe 200). On doit donc comprendre que les souris du groupe 200 ont un nouveau d'anxiété différent des souris du groupe contrôle. Mais les auteurs ne donnent pas les valeurs pour les groupes 400 et 800. Nous pensons que si les conclusions de l'étude sont que l'adjuvant migre plus facilement lorsqu'il est à faible dose, il serait normal de donner aux lecteurs les valeurs obtenues à des doses plus élevées pour comparaison. Dans la présentation de mars 2016, on peut trouver les valeurs pour le groupe 800 (et aussi pour le groupe 133 dont le nombre de cellules microgliales semble d'ailleurs peu différer du groupe contrôle). Étrangement, dans la présentation, la valeur de "p" entre le groupe contrôle et le groupe 200 est très légèrement supérieure à 0.05 (0.056 en fait), ce qui ne serait indicatif que d'une tendance à strictement parler et non d'une différence significative. Dans l'article, p est inférieur à 0.05. Que s'est-il passé entre mars et novembre?
Analyses : la quantité d'aluminium
L'autre moitié des souris doit servir pour une détermination de la quantité d'aluminium présente dans le cerveau. Cette fois, les 5 souris prévues ont bien été utilisées. Les résultats sont exprimés en µg (microgramme) d'aluminum par gramme de tissu cérébral sec (les cerveaux ont subi un procédé de déshydratation avant analyse). Pas de sous-tests. Et cette fois, les résultats sont bien donnés pour les 4 groupes. Le groupe 200 a significativement plus d'aluminium dans le cerveau que le groupe contrôle. Les groupes 400 et 800 (de même que le groupe 133 de la présentation de mars 2016) ne diffèrent pas significativement du groupe contrôle.
Analyses : tissus musculaires
Pour 3 souris de chaque groupe (pourquoi 3 ? Pourquoi pas 5 ou même les 10 ?), une analyse de tissus musculaires est également réalisée en vue de chercher des traces d'inflammation, sous forme de granulomes (agrégat de macrophages). Les résultats sont rangés selon 4 catégories : pas d'inflammation (0 granulome), inflammation + (1 à 3), ++ (au moins 3) ou +++ (au moins 3 grands granulomes), pour les groupes 200, 400 et 800. Le groupe contrôle n'a pas été analysé. C'est dommage mais ça ne change sûrement pas grand chose. Les résultats sont présentés sous forme de tableau mais il n'y pas d'analyse statistique. On ne sait pas ce que l'on doit en conclure. Tout ce qu'on peut dire c'est que le groupe 200 tend à ne pas présenter de granulomes (ce qui serait d'ailleurs cohérent avec la migration de l'adjuvant vers le cerveau observée pour ce groupe), tandis que les groupes 400 et 800 en présentent.
Discussion
L'article finit comme il se doit par une discussion qui présente les conclusions à tirer des résultats et fournit des pistes pour les expliquer.
Les 4 sous-tests de comportements qui permettent de conclure à un effet délétère de la faible dose sur la motricité et l'anxiété (test 1: "open field"), tandis qu'il ne se passe rien à doses intermédiaires et élevées sont mis en avant, ainsi que le sous-test à la "tendance non significative" pour ce qui concerne la force musculaire (test 5: "grip strength"). Aux oubliettes le sous-test qui démontre un effet sur la motricité à la fois dans les groupes 200 et 400. En dehors de cela, nous pensons que les résultats des différents tests ne sont pas spécialement si cohérents que cela entre eux. Si le test "grip strength" montre quelque chose concernant la force musculaire, pourquoi le test "wire mesh hang" ne montre rien ? Si le "open field" montre quelque chose concernant l'anxiété et la motricité, pourquoi les "o-omaze " et "rotarod" ne montrent rien ?
Pour avancer, admettons un instant un effet délétère à la dose 200 seulement en ce qui concerne la motricité, l'anxiété et la force musculaire. Les auteurs avancent que ce résultat est cohérent avec :
- L'analyse de la densité en cellules microgliales dans une des 4 régions du cerveau observées ("ventral forebrain"). Mais comme on n'a pas les chiffres pour les groupes 400 et 800, nous voilà obligés de croire les auteurs sur parole. De plus, cette région du cerveau est présentée comme en rapport avec l'anxiété, qui est bien testée dans le test open field. Mais encore une fois, le test "o maze" qui teste aussi l'anxiété n'avait rien montré. Par ailleurs, quel serait le rapport avec un effet sur la force musculaire alors qu'on n'observe rien au niveau du cortex moteur pour les cellules microgliales ? Quand on y regarde de plus près, ça ne semble plus si cohérent.
- L'analyse de la quantité d'aluminium présent dans le cerveau (alu chez le groupe 200, pas chez les groupes 400 et 800) qui est elle-même cohérente avec le fait qu'il n'y ait pas de granulomes dans les muscles du groupe 200 contrairement aux groupes 400 et 800.
La discussion qui apporte des hypothèses sur le mécanisme de transport depuis le site d'injection vers le cerveau pour le seul cas de la dose faible est intéressante. Mais la question de la neurotoxicité (c'est-à-dire la question des effets délétères sur le comportement) reste, selon nous, en suspens. Déclarer que l'adjuvant est toxique pour les souris nous semble prématuré au vu des résultats des tests comportementaux qui sont moins conclusifs qu'il n'y paraît et au vu de leur manque de cohérence avec les tests sur les cellules microgliales.
Nos conclusions ?
- Absence du cinquième groupe sensé représenter le cas d'un vaccin chez l'humain dans l'article.
- Le protocole de l'étude visait à étudier l'effet de la dose cumulée. Mais les conclusions mettent en avant un effet de la dose unique.
- Possible biais d'observation lors des tests comportementaux (pas de protocole en aveugle).
- Seuls 6 des 36 tests réalisés sur les 40 souris montrent l'une ou l'autre différence significative. Possibilité d'artefacts statistiques.
- Seuls 4 de ces 6 tests sont compatibles avec la conclusion des auteurs qu'il existe une différence significative entre le groupe contrôle et le groupe 200.
- Le 5ème test significatif est mis en avant par les auteurs à cause d'une tendance entre le groupe contrôle et le groupe 200 et non à cause d'une différence significative.
- Le 6ème test significatif, qui ne va pas dans le sens de la conclusion des auteurs, n'est pas discuté.
- Certaines observations des tests de comportement ont peut-être été omises dans l'article.
- Absence des résultats des groupes "400" et "800" pour la densité en cellules microgliales dans le "ventral forebrain".
- Incohérences de certains résultats (tests comportementaux et densité en cellules microgliales) entre l'article et la présentation donnée quelques mois auparavant.
- Seules 3 souris servent aux analyses de cellules microgliales et de tissus musculaires alors que 5 ou 10 souris auraient pu être utilisées.
- Incohérence entre la zone du cerveau affectée par les adjuvants (ventral forebain qui régit l'anxiété) et les résultats des tests comportementaux qui montrent des résultats variés concernant l'anxiété, la motricité et la force musculaire.
Bref, des souris, mais pas de quoi fouetter un chat... A la place de la recommandation des auteurs de réévaluer de la sécurité des adjuvants et des demandes d'associations comme E3M pour retirer les adjuvants aluminiques des vaccins, ils pourraient tout aussi bien conclure qu'il suffirait de mettre une dose suffisamment élevée d'adjuvant dans chaque vaccin pour s'assurer de la sécurité...
Mais peu importe, la machine médiatique continue de tourner. Gherardi vend un livre ("Toxic Story: Deux ou trois vérités embarrassantes sur les adjuvants des vaccins"), est invité à la télé, à la radio... Sa collaboratrice (Guillemette Crépeaux), première auteure de l'étude sur les souris dont nous avons parlé plus haut voudrait même faire croire, par voie de presse, que l'ANSM cache des rapports pour étouffer leurs travaux (après les avoir financés ? Et alors que les études sont publiées dans des revues internationales ? Sérieusement...). La réaction de l'ANSM ne s'est pas fait attendre.
Et pendant ce temps, les craintes des parents français augmentent avec ce que cela peut entraîner en termes d'influence sur les couvertures vaccinales... Ce qui ne paraît pas être une grande préoccupation de l'association E3M et de Gherardi.
Nous remercions la Théière Cosmique pour leurs commentaires sur une version antérieure de ce billet

/image%2F0426111%2F20140915%2Fob_344e7c_logo.jpg)
/image%2F0426111%2F201302%2Fob_12a9121560dfa48fd9c8bbb29933d8e9_monde-rougeole3.PNG)